Une nouvelle maladie touchant les dromadaires du désert algérien a été détectée en 2018 : les Touaregs et autres nomades du désert pourraient-ils un jour se voir privés de leur animal fétiche qui leur sert à la fois de moyen de déplacement, de transport de marchandises et de source de nourriture ? Mohammed Moudjou, chercheur au sein de la task-force « Prion » de l’Inra, apporte son éclairage dans un article rédigé pour The Conversation.
Une nouvelle maladie touchant les dromadaires du désert algérien a été détectée en 2018 : les Touaregs et autres nomades du désert pourraient-ils un jour se voir privés de leur animal fétiche qui leur sert à la fois de moyen de déplacement, de transport de marchandises et de source de nourriture ?
La maladie en question a déjà sévi en Europe, et plus particulièrement au Royaume-Uni dans les années 1985-2010. Il s’agit de l’encéphalopathie spongiforme bovine (ESB), une maladie à prion plus connue sous le nom de « maladie de la vache folle ». Une autre maladie à prion a aussi été détectée récemment chez les cervidés dans les pays scandinaves depuis avril 2016.
À lire aussi : La saga du prion : après la vache folle, les élans et les rennes fous ?
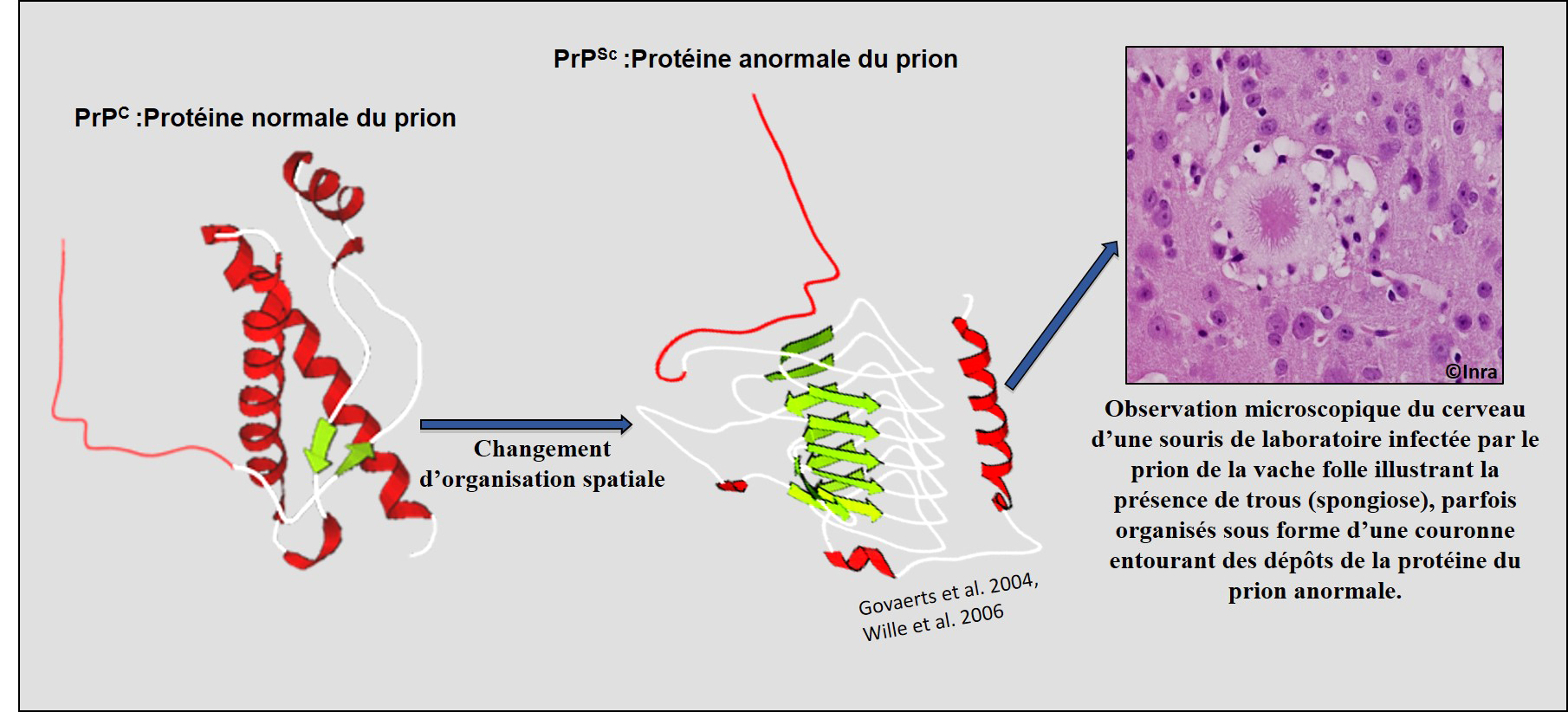
Les prions sont des agents pathogènes non conventionnels : l’agent infectieux n’est ni un virus ni une bactérie, mais correspond à une protéine dont l’organisation spatiale est anormale. La protéine du prion existe dans un état normal chez les individus et les animaux sains ; lorsqu’elle se transforme pour des raisons et par des mécanismes non encore complètement élucidés, elle s’accumule sous la forme de particules protéiques agrégées toxiques pour les cellules du système nerveux. Les maladies à prion font partie de la famille des maladies du mauvais repliement des protéines, à l’instar des maladies d’Alzheimer et de Parkinson.
Trois premiers dromadaires malades en 2018
Grâce aux recherches et à l’acharnement de deux chercheurs algériens, Baaissa Babelhadj, vétérinaire de l’université de Ouargla et Semir Bechir Suheil Gaouar, chercheur en génétique moléculaire à l’université de Tlemcen, les premiers cas de dromadaires touchés par un prion ont été reportés en 2018. Il s’agit de trois animaux âgés de 11 à 14 ans.
Dès 2014, les deux chercheurs avaient commencé à observer des cas de dromadaires destinés à l’abattage présentant des comportements et des symptômes particuliers : hyperactivité, tremblements, grincement de dents, agressivité, mouvements répétitifs et anormaux de la tête, démarche chancelante, perte de contrôle des membres, chutes occasionnelles et difficultés à se lever. La maladie évoluait vers un décubitus et la mort des animaux en 3 à 8 mois.
Selon les deux scientifiques, 3,1 % des dromadaires envoyés à l’abattoir de Ouargla entre 2015 (20 cas sur 937) et 2016 (51 cas sur 1 322) présentaient ces symptômes, ce qui correspond à une fréquence assez élevée. D’après une enquête rétrospective auprès des éleveurs et le personnel d’abattoirs, de tels symptômes auraient été observés dès les années 1980.
Une nouvelle forme de prion découverte
L’analyse des encéphales des camélidés infectés a permis d’identifier une nouvelle forme de prion appelée « camel-prion disease ». Une étude approfondie a été engagée avec le laboratoire de référence européen des maladies à prion à Rome et a conduit à une publication dans la revue scientifique Emerging Infectious Diseases en 2018. Pour des raisons obscures, ceci a valu aux deux scientifiques algériens et au ministère de l’Enseignement supérieur un avertissement de la part du ministère de l’Agriculture.
Il s’agit de la première description d’une maladie à prion chez les camélidés dans le monde. Son origine est totalement inconnue à ce stade des investigations. L’Algérie est un pays dit indemne d’autres formes de maladies à prions animales (vache folle, tremblante du mouton et de la chèvre). Mais cela ne garantit pas l’absence de ces maladies du territoire. En effet, pas ou peu de tests sont réalisés, et il n’y a pas d’informations sur l’existence d’une réelle surveillance clinique. Il est néanmoins utile de rappeler ici que si l’Angleterre a interdit les farines animales en 1988 après la découverte de l’ESB dans son cheptel (les farines animales étant le vecteur de transmission de l’ESB au sein des bovins), elle a continué à les exporter vers les pays étrangers. Les pays en voie de développement ont ainsi importé plus de 30 000 tonnes de ces farines jusqu’en 1991.
Ce qui est inquiétant dans l’histoire du camel-prion, c’est sa distribution dans des organes périphériques lymphoïdes (rate, ganglions lymphatiques), en plus du système nerveux central. Ceci souligne une forme infectieuse de la maladie dont le pouvoir de dissémination pourrait être important, à l’instar de ce qui est documenté pour la tremblante du mouton, la maladie du dépérissement chronique (MDC) des cervidés ou pour le variant de la maladie de Creutzfeldt-Jakob (ESB chez l’homme).
Un risque potentiel de transmission à l’humain
Le risque pour les populations autochtones, du fait de la consommation de viande, de lait et d’autres tissus est à considérer sérieusement étant donné le pouvoir de franchissement de la barrière d’espèce de ces pathogènes atypiques.
Selon l’Organisation des Nations unies pour l’alimentation et l’agriculture, la population de camélidés dans le monde est estimée à 28 millions d’animaux, dont 88 % vivent en Afrique.
L’Algérie compte près de 350 000 dromadaires, répartis dans trois grandes régions d’élevage (sud-est, sud-ouest et extrême sud) ; les effectifs ayant nettement augmenté depuis le début des années 2000. Cet élevage représente un intérêt économique, social et culturel dans le pays. La présence d’un prion dont la dissémination pourrait être très efficace représente un réel danger pour ce patrimoine saharien. Il serait alors utile d’évaluer assez rapidement l’incidence réelle de cette nouvelle pathologie, et d’identifier son origine en Afrique.
Une origine encore mystérieuse
D’où le camel-prion peut-il bien provenir ? S’agit-il d’une forme spontanée spécifique aux dromadaires ? Est-il issu d’une forme dérivée d’une autre espèce après consommation de produits contaminés par d’autres prions (tremblante, ESB) ? Quant à la probabilité d’une contamination iatrogène (acquise suite à un traitement médical), elle reste faible du fait de l’absence de programmes de vaccination chez les dromadaires. En effet, des moutons vaccinés en Écosse et en Italie par des vaccins contaminés par l’agent de la tremblante a provoqué une épidémie dans les cheptels écossais au milieu des années 1930 et italiens en 1997.
L’hypothèse d’une contamination alimentaire a été étayée par l’un des chercheurs dans un entretien accordé au HuffPost :
« Nous ne sommes pas encore sûrs de cela, mais il se pourrait que ce soit le changement de régime alimentaire des dromadaires qui ait causé l’apparition de cette maladie, mon collègue le Dr. Babelhadj m’a envoyé des photos de chameaux, non loin d’une base-vie, en train de manger des saucisses… alors que nous savons tous que les chameaux ne mangent que l’herbe habituellement ».
Cependant, les caractéristiques biochimiques de la protéine prion infectieuse identifiée dans le cerveau des dromadaires sont différentes de celles de la tremblante classique ou de l’ESB. Les expériences en cours (inoculation à des souris de laboratoire) apporteront des éléments de réponse quant au risque de franchissement de la barrière entre espèces, plus particulièrement le risque zoonotique (transmission à l’humain).
Des mesures nécessaires pour enrayer la maladie
Afin de prévenir la transmission de la maladie à court terme, des mesures d’épidémiosurveillance active doivent être mises en place dans les pays où l’élevage et la consommation de produits issus de camélidés (Afrique, Moyen-Orient…) est monnaie courante. Une autre démarche qui a déjà été entreprise par les chercheurs algériens consiste à étudier le gène de la protéine du prion normal des dromadaires afin de savoir s’il existe des génotypes résistants à cette maladie, comme cela a été décrit chez d’autres espèces (mouton, chèvre, humain).
Une sélection génétique des animaux résistants pourrait mettre fin au camel-prion. Il faudra alors espérer que d’autres souches de prion ne surgissent et ne s’adaptent, comme ce fut le cas pour la tremblante du mouton atypique appelée Nor98 identifiée par Sylvie Benestad en Norvège en 1998.
Comme pour la maladie touchant les cervidés des Lapons et au-delà des considérations économiques, il est essentiel de réagir face à ces nouveaux pathogènes émergents qui touchent un patrimoine ancestral de l’humanité et menacent d’autres espèces animales.
Cet article est republié à partir de The Conversation sous licence Creative Commons. Lire l’article original.